发布日期:2024-12-06 作者: 检测能力
B.磁性氧化铁为四氧化三铁,溶于盐酸后生成铁离子和亚铁离子,离子方程式:Fe
点评本题考察了离子方程式的正误判别,为高考中的高频题,把握离子方程式的书写准则,清晰离子方程式正误判别常用办法:查看反响物、生成物是不是正确,查看各物质拆分是不是正确,如难溶物、弱电解质等需求保存化学式,查看是不是契合守恒联系即可回答,标题难度中等.
化学试验的微型化可有效地削减污染,完成化学试验绿色化的要求.某学生按下列操作做一个试验:在一块下衬白纸的玻璃片的不同方位别离滴加浓度为0.1mol/L的KBr、KI(含淀粉溶液)、NaOH(含酚酞)、FeCl
(含KSCN)溶液各1滴,每种液滴互相分隔,围成半径小于表面皿的圆形(如下图所示),在圆心处放置2粒芝麻粒巨细的KMnO
(1)e处反响的离子方程式为2MnO4-+16H++10Cl-═2Mn2++5Cl2↑+8H2O,该反响中产生反响的氧化剂和还原剂的物质的量之比为1:5.
(2)b处的试验现象为溶液由无色变为蓝色,d处的试验现象为溶液变为赤色.
(4)通过该试验能否比较Cl2、FeCl3、KMnO4三种物质氧化性的强弱?能(填“能”或“不能”),若能,其氧化性由强到弱的次序是KMnO4>Cl2>FeCl3.
(1)“绿色化学”的最大特色在于它是在始端就选用防备试验污染的科学手法,因此进程和终端均为零排放和零污染,具有“原子经济性”.下列化学反响不契合“绿色化学”思维的是BD;
(2)冶金废水中含有[Au(CN)2]-,其电离出的CN-有毒,当与H+结合生成HCN时,其毒性更强.工业上处理这种废水是在碱性条件下,用NaClO将CN-氧化为CO32-和一种无毒气体,该反响的方程式为5ClO-+2CN-+2OH-=2CO32-+N2↑+5Cl-+H2O,在酸性条件下,ClO-也能将CN-氧化,但实践处理时却不在酸性条件下进行的根本原因在酸性条件下,CN-与H+结合生成毒性很强的HCN,对人和环境可以形成损害;
(3)工业上现在运用两种办法制取乙醛--“乙炔水化法”和“乙烯氧化法”.下面两表供给出产的悉数进程中质料、反响条件、质料平衡转化率和产值等的有关信息:
①从产率和产值视点剖析尽管乙烯氧化法的转化率略小于乙炔水化法,但反响快、日产值比其高得多;
②从环境保护和能耗视点剖析两者反响条件温度适当,但乙炔水化法制乙醛运用的是汞盐催化剂,毒性大;乙炔的制取要通过多步反响制得,且耗费很多的热能、电能;乙烯来源于石油裂解气,耗费的总能量比乙炔少,且较简单取得.
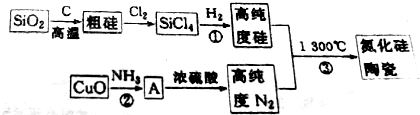
(1)SiO2和C反响除了得到粗硅外,还有或许得到一种硬度也很大的物质,是生成粗硅仍是生成该物质主要是由C的用量决议的.
版权所有© 2018 爱游戏|爱游戏官网打开|爱游戏登录网页入口 豫ICP备06005967号-2 网站地图