发布日期:2024-12-31 作者: 检测能力
(1)制造待测液:用5.0g含有少数杂质(杂质不与盐酸反响)的固体烧碱样品制造1000mL溶液.除烧杯外,还需求的玻璃仪器有
(2)滴定:①盛装0.1000mol?L-1盐酸规范液应该运用式滴定管.
④先算出两次耗费盐酸的均匀体积,然后求出氢氧化钠的物质的量,再核算烧碱样品的纯度;
(5)酸性高锰酸钾具有强氧化性和酸性.回答:解:(1)制造1000mL必定物质的量浓度的氢氧化钠溶液需求仪器:1000mL容量瓶、胶头滴管、烧杯、玻璃棒、天平、药匙,所以制造待测液还需求的玻璃仪器有1000mL容量瓶、玻璃棒、胶头滴管,烧杯;
③用盐酸滴定氢氧化钠溶液,酚酞滴在氢氧化钠溶液中,显赤色,当到达滴定结尾时溶液由浅赤色变为无色,而且半分钟内不褪色;
(4)①冲刷锥形瓶,不影响待测物NaOH的总物质的量,不会影响测定成果;故答案为:无影响;
②滴定进程中不小心将酸滴在瓶外,耗费盐酸的体积偏多,则测定成果偏大,故答案为:偏高;
③滴定前仰望、滴定后仰望,耗费盐酸体积偏小,则测定成果偏小,故答案为:偏低;
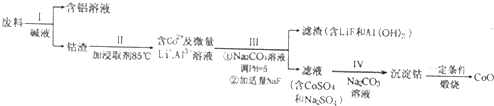
(2)进程Ⅱ酸化,再参加Na2S2O3溶液浸出钴(已知反响后的溶液中只要一种酸根离子),写出浸出钴的离子方程式.
(3)进程Ⅲ参加Na2CO3溶液在沉积铝时起到及其重要的效果,写出其反响的离子方程式.
mol/L的Na2CO3溶液中逐滴参加0.1mol/LCoSO4溶液,开端生成的沉积为(写化学式).工艺流程中进程Ⅳ生成沉积的离子方程式为.
版权所有© 2018 爱游戏|爱游戏官网打开|爱游戏登录网页入口 豫ICP备06005967号-2 网站地图