发布日期:2025-03-15 作者: 检测能力
B、离子反响方程式遵从电荷守恒,将少数金属钠放人冷水中的反响为2Na+2H
C、亚硫酸钠具有强复原性,能被硝酸氧化,二者产生的是氧化复原反响,故C过错;
D、弄清石灰水中通入过量二氧化碳的反响为:CO2+OH-=HCO3-,故D过错.


(2)C、D、E三种元素构成的简略离子,其离子半径从大到小的次序为N3-、O2-、Na+N3-、O2-、Na+(用离子符号表明).
(3)上述元素的最高价氧化物对应的水化物酸性最强的是HClO4HClO4(写化学式),非金属气态氢化物复原性最强的是H2SH2S(写化学式).
(6)以A2、D2及E的最高价氧化物对应的水化物为首要的组成原资料,能够规划成一种电池,该电池负极的反响为H2+2OH--2e-=2H2OH2+2OH--2e-=2H2O,电池运用的过程中电解质溶液的pH减小减小(填“增大”、“减小”或“不变”).
(2)我国遍及选用一种方法制得含有A、C、E三种元素的某重要化工产品,其工业生成的第一步化学反响方程式为______.
(3)均由A、C、D、E四种元素组成的两种物质在溶液中反响的离子方程式为______.
(4)由A与C两种元素组成的一种化合物能使酸性高锰酸钾褪色,反响的离子方程式是______.
(5)单质B可与由A、C、E三种元素组成的化合物在必定条件下反响生成EC2,该反响的化学方程式为______.
(6)B元素的氢化物有多种,1molB的某种氢化物中含有14mol电子,已知在25℃,101kPa下,1g该气态氢化物在足量氧气中彻底焚烧生成液态水时放出热量为50kJ,写出该物质焚烧热的热化学方程式______.
肼(N2H4)又称联氨,大范围的运用在火箭推进剂、有机组成及燃料电池,NO2的二聚体N2O4则是火箭中常用氧化剂。试答复下列问题
(1)肼燃料电池原理如图所示,左面电极上产生的电极反响式为_________。

![]()
试写出气态肼在气态四氧化二氮中焚烧生成氮气和气态水的热化学方________。
(3)联氨的工业生产常用氨和次氯酸钠为质料取得,写出反响的离子方程式为___。
(4)如图所示,A是由易导热资料制造成的体积不变的密闭容器,B是一耐化学腐蚀且易于传热的体积可变的通明气囊(体积改动过程中囊体弹力改动忽略不计)。封闭K2,将各1 mol NO2经过K1、K3别离充入A、B中,反响开始时A、B的体积相同均为a L。

![]()
②若翻开K2,平衡后B容器的体积缩至0.4a L,则翻开K2之前,气球B体积为______L。
③若容器A中抵达平衡所需时刻t s,抵达平衡后容器内压强为开始压强的0.8倍,则 均匀化学反响速率v(NO2)等于____________________(用含a、t的代数式表明)。
④若平衡后在A容器中再充入0.5mol NO2,则从头抵达平衡后,平衡混合气中NO2的体积分数_______________(填 “变大”“变小”或“不变”)。
肼(N2H4)又称联氨,大范围的运用在火箭推进剂、有机组成及燃料电池,NO2的二聚体N2O4则是火箭中常用氧化剂。试答复下列问题
(1)肼燃料电池原理如图所示,左面电极上产生的电极反响式为_________。
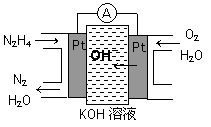
![]()
试写出气态肼在气态四氧化二氮中焚烧生成氮气和气态水的热化学方________。
(3)联氨的工业生产常用氨和次氯酸钠为质料取得,写出反响的离子方程式为___。
(4)如图所示,A是由易导热资料制造成的体积不变的密闭容器,B是一耐化学腐蚀且易于传热的体积可变的通明气囊(体积改动过程中囊体弹力改动忽略不计)。封闭K2,将各1 mol NO2经过K1、K3别离充入A、B中,反响开始时A、B的体积相同均为a L。
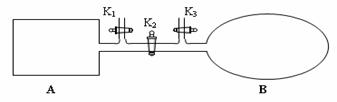
![]()
②若翻开K2,平衡后B容器的体积缩至0.4a L,则翻开K2之前,气球B体积为______L。
③若容器A中抵达平衡所需时刻t s,抵达平衡后容器内压强为开始压强的0.8倍,则 均匀化学反响速率v(NO2)等于____________________(用含a、t的代数式表明)。
④若平衡后在A容器中再充入0.5mol NO2,则从头抵达平衡后,平衡混合气中NO2的体积分数_______________(填 “变大”“变小”或“不变”)。
版权所有© 2018 爱游戏|爱游戏官网打开|爱游戏登录网页入口 豫ICP备06005967号-2 网站地图